Hej, jeg er ved at lave nogle opgaver i kemi…
Jeg har lidt problemer med følgende opgave:
Hvilken ladning har aminosyren glutamin ved et neutralt pH?
Facit siger at ladningen er neutral, hvilket jeg ikke kan forstå.
Jeg har slået op at det isoelektriske punkt for glutamin er pHiso= 3,08. Derudover er pK1= 2,1. pK2= 4,07. pK3 = 9,47.
Jeg ville da sige at ladningen er negativ. Mellem pK1 og pK2 burde ladningen da være neutral da det er imellem disse to pK værdier at det isoelektriske punkt er… eller hvad ?
Håber der er nogen der kan forklare mig dette, da jeg er stødt på rimelig mange lignende spørgsmål og har slet ikke kunnet finde ud af dem 
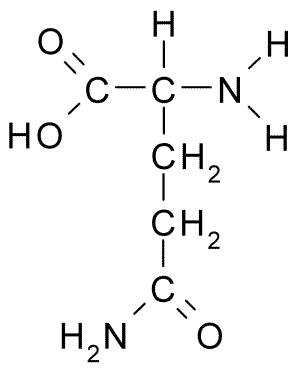
Dobbeltbindingen du ser ved O, fluktuerer faktisk mellem O og NH2. NH2 er polært ved neutral pH, men er for svag en base til at den vil optage nogen elektroner ved neutral pH (da den på en måde deler lidt med O). Sådan husker jeg hvertfald at få det forklaret. Håber det hjalp
Facit har ret. Glutamin er neutralt ved pH 7.
De pKa-værdier du opgiver har jeg ikke tjekket, men svaret er:
Syregruppen COOH er deprotoneret (altså negativ, COO-) ved pH 7, mens aminen (R-NH2) stadig er protoneret (altså positiv, R-NH3+). Amidet påvirkes ikke, da det ikke rigtigt har syre-baseegenskaber pga. resonansstabilisering med carbonylgruppen, og forbliver derfor neutralt.
Det vil sige: Der er en positiv ladning (amin) og en negativ ladning (syren), hvilket udligner hinanden og giver et neutralt molekyle, en såkaldt zwitterion.

